FDA schvaluje generický Lexapro pro depresi, úzkost
Americký úřad pro kontrolu potravin a léčiv ve středu schválil první generický přípravek Lexapro (tablety escitalopramu) k léčbě deprese i generalizované úzkostné poruchy u dospělých.
Lexapro je jedním z nejčastěji předepisovaných psychiatrických léků v USA, v článku z roku 2009 od IMS Health (citovaného na ), který je druhý za anxiolytickým přípravkem Xanax (alprazolam).
Deprese je charakterizována příznaky, které narušují schopnost člověka pracovat, spát, studovat, jíst a užívat si jednou příjemné činnosti. Epizody deprese se často opakují po celý život člověka.
Známky a příznaky závažné deprese zahrnují: depresivní náladu, ztrátu zájmu o obvyklé činnosti, změnu hmotnosti nebo chuti k jídlu, nespavost nebo nadměrné spaní (hypersomnie), neklid, zvýšenou únavu, pocity viny nebo bezcennosti, zpomalené myšlení nebo poruchy soustředění a pokusy o sebevraždu nebo myšlenky na sebevraždu.
Lidé s generalizovanou úzkostnou poruchou (GAD) jsou naplněni přehnanými obavami a napětím, i když je jen málo nebo nic, co by to provokovalo. Předvídají katastrofu a jsou příliš znepokojeni zdravotními problémy, penězi, rodinnými problémy nebo obtížemi v práci. GAD je diagnostikována, když se člověk po dobu nejméně šesti měsíců nadměrně obává různých každodenních problémů. Lidé s GAD mají potíže s uvolněním a soustředěním.
"Tyto psychiatrické stavy mohou být znemožňující a mohou člověku bránit v každodenních činnostech," uvedla Janet Woodcock, MD, ředitelka Centra FDA pro hodnocení a výzkum drog. "Tento lék je široce používán lidmi, kteří musí časem zvládat svůj stav, takže je důležité mít dostupné možnosti léčby."
Společnosti Teva Pharmaceutical Industries / IVAX Pharmaceuticals získaly souhlas FDA pro prodej generického escitalopramu v silách 5 mg, 10 mg a 20 mg.
V klinických studiích s přípravkem Lexapro byly nejčastěji pozorovanými nežádoucími účinky: nespavost (nespavost), porucha ejakulace, nevolnost, zvýšené pocení, únava a ospalost a nízký sexuální apetit (snížené libido).
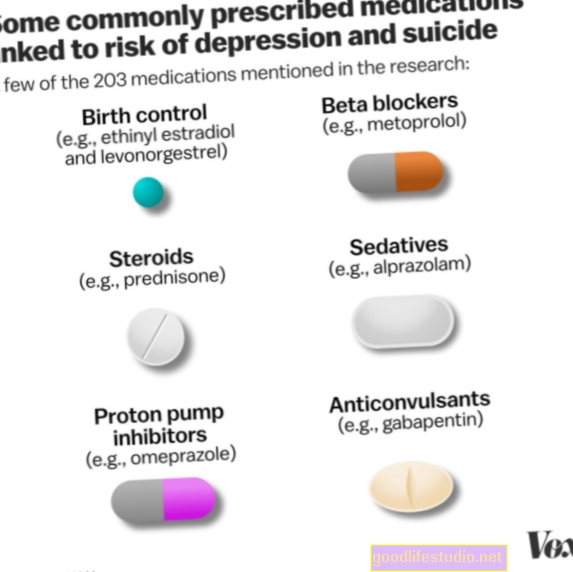
Escitalopram a všechny ostatní antidepresiva mají krabicovou výstrahu a příručku pro léčbu pacientů popisující zvýšené riziko sebevražedného myšlení a chování u dětí, dospívajících a mladých dospělých ve věku od 18 do 24 let během počáteční léčby.
Varování také říká, že údaje neukazují toto zvýšené riziko u osob starších 24 let a že pacienti ve věku 65 let a starší, kteří užívají antidepresiva, mají snížené riziko sebevražedného myšlení a chování. Varování říká, že deprese a další závažné psychiatrické poruchy jsou samy o sobě nejdůležitějšími příčinami sebevraždy a že je nutné pečlivé sledování pacientů, kteří začínají s těmito léky.
Společnost Teva získala 180denní období exkluzivity generických léků, což znamená, že FDA nemůže před koncem tohoto období schválit další generickou verzi tablet escitalopramu. Obecná léčiva schválená FDA mají stejně vysokou kvalitu a sílu jako značková léčiva. Generické výrobní a balicí závody musí splňovat stejné standardy kvality jako standardní značkové léky.
Zdroj: US Food and Drug Administration