FDA pro farmaceutické společnosti: Použití mimo označení Ok
Lékaři byli vždy schopni předepsat jakoukoli drogu, kterou chtějí, na cokoli chtějí. Farmaceutickým společnostem však bylo povoleno inzerovat a prodávat pouze léky, které byly schváleny FDA pro konkrétní použití nebo poruchy. To znamená, že antidepresivum lze obecně prodávat a propagovat pouze na depresi. Pokud chce společnost uvádět na trh a propagovat svůj lék pro jiné účely, musí se vrátit zpět k Úřadu pro kontrolu potravin a léčiv (FDA) v USA a podat další aplikace s bohatou podporou výzkumu na podporu těchto použití.
Pokud výzkum není silný a trh není potenciálně lukrativní, mnoho farmaceutických společností se rozhodne omezit množství dalších použití, o která žádají schválení FDA.
Jakékoli použití léku, které nezískalo schválení FDA, je považováno za „off-label“ v tom smyslu, že se nejedná o použití, které není na štítku drogy.
Jak tedy lékaři vědí, jaké léky mají předepisovat off-label za jakých podmínek? Mohli by o tom slyšet na konferenci (další lékařské vzdělávání nebo CME, o které bloguje Dr. Carlat často nepřímo financované nebo sponzorované farmaceutickými společnostmi), nebo si o tom přečíst v oblíbeném lékařském časopise.
Ale farmaceutické společnosti dlouho považovaly takovou metodu za poměrně nespolehlivou.
Co kdyby FDA řekla farmaceutickým společnostem, že by mohly pomoci vzdělávat lékaře o těchto off-label použitích?
The Wall Street Journal má příběh, Zvyšte užívání drog mimo značku:
Úřad pro kontrolu potravin a léčiv chce umožnit farmaceutickým společnostem poskytovat lékařům informace o neschváleném užívání léků na předpis, což je kontroverzní krok, který již nyní vznáší námitky od Capitol Hill. […]
Regulační orgán vstupuje do obchodní oblasti s vysokými sázkami, protože off-label užívání léků na předpis je oporou průmyslu - podle analýzy zveřejněné v roce 2006 odhadem 21% celkového užívání drog Archiv vnitřního lékařství.
Zdánlivě chce FDA zveřejnit takové pokyny, které by pomohly regulovat temnou oblast marketingu drog a řešily toto běžné používání receptů.
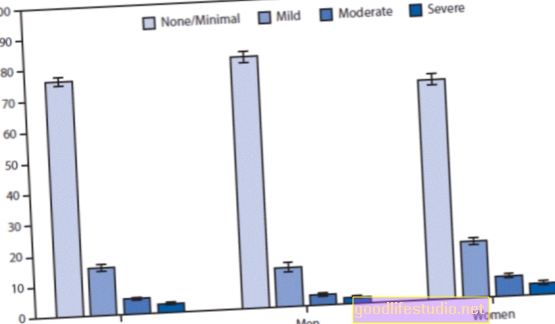
Pětina všech léků je již předepisována off-label a mezi psychiatrickými léky stoupá na 31% (Radley, et. Al. 2006) - jeden ze tří psychiatrických léků je předepisován pro použití, které není schváleno FDA . Ale nejde o nové zprávy a domnívám se, že skutečný počet je ještě vyšší.
Skutečným problémem při užívání mimo značku je, že má méně důkazů a důkazů nižší kvality, které podporují předepisování drogy. V Radley et. al. (2006) zjistili:
Ne více než 30% off-label praktik, které jsme pozorovali, bylo podpořeno silnými vědeckými důkazy.
To znamená, že v 70% údajů, které analyzovali - drtivá většina - lékaři psali recepty na užívání drog mimo značku s minimálními empirickými důkazy na podporu tohoto předpisu.
Což je naprosto v pořádku, protože je výsadou lékaře, aby k vypracování takových receptů použil svůj vlastní, individuální klinický úsudek.
Co se ale stane, když necháme farmaceutické společnosti, které mají silný finanční zájem a vlastní předpojatost, prodávat své léky pro jakékoli a mimopovolené použití, a to s použitím minimálních důkazů (např. Jediná zveřejněná případová studie)?
Myslíme si, že je nevhodné, aby FDA umožňovala farmaceutickým společnostem propagovat tato další off-label použití léků přímo lékařům, protože (a) takové použití má mnohem méně přísná klinická data na podporu takové rozšířené propagace; b) potenciál zneužití tohoto marketingu pro lékaře je prostě příliš vysoký; a (c) marketingová oddělení farmaceutických společností prokázala nerovnoměrnou historii jednání v nejlepším zájmu bezpečnosti pacientů nebo skutečné účinnosti léku. Pokud chce FDA vyjasnit tuto temnou oblast svých předpisů, měla by to klidně udělat, ale ne otevřením ještě více marketingových příležitostí pro společnosti.
Chcete si přečíst více? Navrhujeme, aby FDA společnosti Merrill Goozner navrhovala zásady medicíny založené na nedostatku důkazů.
Odkaz:
Radley DC, Finkelstein SN, Stafford RS. (2006). Off-label prescription mezi kancelářskými lékaři. Arch Intern Med., 166 (9), 1021-6.