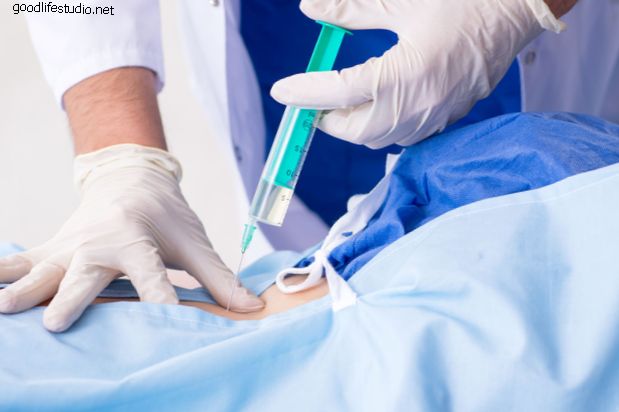
Celexa souvisí s poškozením srdce při vysokých dávkách
FDA vydala varování pro zdravotnické pracovníky, protože vědci zjistili, že Celexa může způsobit abnormální změny v elektrické aktivitě srdce, pokud se užívá ve vyšších dávkách - což vede k možnému poškození srdce. Předchozí vědecké studie přípravku Celexa neprokázaly přínos při léčbě deprese při dávkách vyšších než 40 mg denně.
Celexa (citalopram hydrobromid) je typ antidepresiva nazývaného selektivní inhibitory zpětného vychytávání serotoninu (SSRI), které běžně předepisují lékaři a psychiatři pro klinickou depresi. Zatímco vědci přesně nevědí, jak antidepresiva působí na snižování deprese, předpokládá se, že působí zvýšením množství chemického neurotransmiteru serotoninu v mozku. V USA je v současné době k dispozici v 10 mg, 20 mg a 40 mg tabletách a je k dispozici také jako perorální roztok (10 mg / 5 ml).
Dříve štítek s léčivým přípravkem na přípravku Celexa uváděl, že někteří pacienti mohou vyžadovat dávku 60 mg denně. Předpokládá se, že lékaři vydali mnoho předpisů pro přípravek Celexa v této vyšší dávce.
Nové varování přichází, když vědci FDA přezkoumali předchozí výzkum a našli přímou korelaci mezi vyšší dávkou přípravku Celexa a větším rizikem pro srdce.
Změny v elektrické aktivitě srdce (prodloužení QT intervalu na elektrokardiogramu [EKG]) mohou vést k abnormálnímu srdečnímu rytmu, který může být fatální.
Mezi pacienty se zvláštním rizikem rozvoje prodloužení QT intervalu patří pacienti se základními srdečními chorobami a pacienti s predispozicí k nízkým hladinám draslíku a hořčíku v krvi.
Byl revidován štítek s citalopramem, aby zahrnoval nová doporučení ohledně dávkování a užívání léků, stejně jako informace o možném prodloužení QT intervalu a Torsade de Pointes. (Viz Další informace pro zdravotnické pracovníky)
Pokud nyní používáte Celexu, je důležité si uvědomit následující:
- Nepřestávejte užívat citalopram ani neměňte dávku bez porady s lékařem. Náhlé zastavení citalopramu může způsobit nežádoucí vedlejší účinky.
- Pokud v současné době užíváte dávku citalopramu vyšší než 40 mg denně, poraďte se se svým lékařem o změně dávky.
- Okamžitě vyhledejte okamžitou péči, pokud během užívání citalopramu zaznamenáte nepravidelný srdeční rytmus, dušnost, závratě nebo mdloby.
- Pokud užíváte citalopram, může váš lékař příležitostně objednat elektrokardiogram (EKG, EKG) ke sledování vaší srdeční frekvence a rytmu. EKG je test, který kontroluje problémy s elektrickou aktivitou vašeho srdce.
- Pečlivě si přečtěte Příručku k léčbě citalopramu a jakékoli otázky, které máte, prodiskutujte se svým lékařem.
FDA řekl zdravotníkům, kteří předepisují přípravek Celexa, že způsobuje prodloužení QT intervalu závislé na dávce. Varovali, že lék by již neměl být předepisován v dávkách vyšších než 40 mg denně, ani by neměl být používán u pacientů s vrozeným syndromem dlouhého QT.
U pacientů s městnavým srdečním selháním, bradyarytmiemi nebo predispozicí k hypokalemii nebo hypomagnezémii z důvodu souběžného onemocnění nebo léků je vyšší riziko vzniku Torsade de Pointes.
FDA také poznamenal, že před podáním citalopramu by měla být upravena hypokalémie a hypomagnezemie. Elektrolyty by měly být monitorovány, jak je klinicky indikováno. Řekli zdravotnickým pracovníkům, aby zvážili častější monitorování elektrokardiogramu (EKG) u pacientů s městnavým srdečním selháním, bradyarytmiemi nebo u pacientů užívajících současně léky, které prodlužují QT interval.
Proč FDA vydalo toto varování ohledně společnosti Celexa
FDA obdržela po uvedení na trh zprávy o prodloužení QT intervalu a Torsade de Pointes spojené s přípravkem Celexa a jeho generickými ekvivalenty.
Kromě toho FDA vyhodnotila výsledky důkladné studie QT hodnotící účinky dávek 20 mg a 60 mg citalopramu na QT interval u dospělých. V této randomizované multicentrické, dvojitě zaslepené, placebem kontrolované zkřížené studii dostávalo 119 pacientů citalopram 20 mg denně (den 9), citalopram 60 mg denně (den 22) a placebo. Celkový souhrn nálezů je uveden v tabulce 1
Ve srovnání s placebem bylo maximální průměrné prodloužení v individuálně korigovaných QT intervalech 8,5 a 18,5 milisekund (ms) pro citalopram 20 mg, respektive 60 mg. U 40 mg citalopramu bylo prodloužení korigovaného QT intervalu odhadnuto na 12,6 ms.
Na základě této důkladné studie QT stanovila FDA, že citalopram způsobuje prodloužení QT intervalu závislé na dávce a neměl by se nadále používat v dávkách vyšších než 40 mg denně. Do příbalových informací o přípravku Celexa a jeho generických ekvivalentech se přidávají důležité bezpečnostní informace o možném prodloužení QT intervalu a doporučení Torsade de Pointes s dávkováním a použitím léku.
Zdroj: US Food and Drug Administration